Comment le savon mousse-t-il ?
DIVERS
+ DE 2 ANS
Le 26/04/2018 à 08h59
301 vues
Question d'origine :
Bonjour,
J'aimerais savoir pourquoi et comment la savon peut-il mousser ? Est-ce qu'un savon maison moussera-t-il autant ?
merci !
Réponse du Guichet
Le 28/04/2018 à 10h00
Bonjour,
Voici les précisions que nous trouvons dans cet article du Figaro bien nommé : Pourquoi le savon mousse-t-il ? :
« Sans vouloir la faire mousser à mauvais escient, force est de reconnaître quetout est dans la bulle . Elle est la pierre angulaire d'un monde étrange et déroutant. Surtout pour les scientifiques. Les lois de la physique et de la chimie qui régissent son existence lui donnent d'ailleurs un physique à nul autre pareil. Car la bulle trompe bien son monde. Un exemple : on la croit ronde comme une sphère ce qu'elle est lorsqu'elle est seule alors que, la plupart du temps, elle préfère adopter l'apparence d'un cube dans la mousse. Et sous son apparence fine et fragile, la bulle cache des trésors d'ingéniosité. Elle est l'une des fées de la matière dite molle, à la fois solide et liquide : elle forme des mousses capables de conserver leur forme hors de tout récipient, mais aussi de couler quand on leur demande. Une bulle, c'est avant tout de l'air, ou un autre gaz, enfermé dans une fine membrane . Dans le cas de la mousse issue des savons et détergents, la peau de la bulle est composée de molécules qui ressemblent, vues de près, à des épingles, avec une tête ronde et une longue pointe . La tête a une attirance irrépressible pour l'eau dans laquelle elle adore se plonger tandis que l'extrémité de leur pointe refuse d'y tremper le moindre bout d'orteil . En présence d'eau, ces molécules-épingles vont donc toutes mettre leur tête dans l'eau et, en se serrant les unes aux autres, elles vont créer un fin film souple capable de se refermer en emprisonnant un gaz ou d'autres corps. Et le savon est précisément très riche en ces molécules-épingles, véritables missiles à tête chercheuse de tout ce qui est gras . »
Science étonnante apporte de son côté une réponse complète à votre question en expliquant comment se comportent les molécules de savon et comment, au contact de l’air, elles créent des bulles (et donc de la mousse). Par ailleurs, cet article confirme qu’un savon naturel ou maison moussera moins qu’un savon industriel (sans pour autant que ses propriétés lavantes soient moindres) :
« le savon […] contient desmolécules qui permettent de réconcilier l’eau et le gras . On les appelle molécules amphiphiles , car elles aiment les deux à la fois : une partie de leur structure est hydrophile , tandis qu’une autre est lipophile (et donc hydrophobe). […]
Grâce à cette propriété, les molécules amphiphiles peuvent alors emprisonner les graisses à la surface de notre peau (ou de nos assiettes), et permettre qu’on les élimine par un flux d’eau. […]
Et d’où vient la mousse ?
Comme vous avez pu le constater,le mécanisme par lequel le savon nous lave ne fait en rien appel à l’existence de mousse . Ca n’est pas la mousse qui nous lave ! En fait la mousse est un effet collatéral des molécules amphiphiles.
Tout d’abord, vous savez peut être qu’il n’y a pas vraiment besoin de savon pour faire des bulles. Si vous faites sortir rapidement de l’eau du robinet, vous pouvez constater que quelques bulles se forment brièvement, mais ont une durée de vie bien faible. Pas de quoi en faire une mousse.
La raison de la faible durée de vie de ces bulles, c’est que tout comme l’huile, l’eau et l’air ne s’aiment pas vraiment. Ils ont donc envie de minimiser leur interface; or une bulle est une grande surface d’interface entre l’eau et l’air. C’est pour cette raison que les bulles créées sans savon ne sont pas stables.
Mais de même que les molécules amphiphiles permettent de rendre compatibles l’eau et l’huile, elles permettent de conserver les bulles en réconciliant l’eau et l’air. Les molécules amphiphiles se placent à l’interface eau-air (la tête dans l’eau et la queue en l’air) et assurent la stabilité du mince film d’eau qui constitue la bulle.
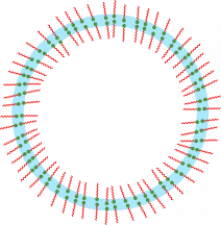
L’image ci-contre représente ce qu’est une bulle, c’est-à-dire une double couche de molécules amphiphiles qui stabilisent un mince film d’eau. Attention tout cela n’est pas à l’échelle car le film d’eau ne fait que quelques dizaines de nanomètres d’épaisseur !
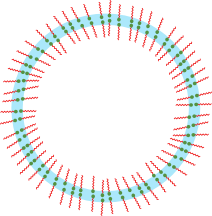
Et voilà pourquoi les produits nettoyants sont aussi inéluctablement des produits moussants ! En réalité, suivant leur structure, les molécules amphiphiles peuvent être plus efficaces à l’interface eau/huile (on parle alors de détergents) ou à l’interface eau/air (on parle alors d’agents moussants).
Mais dans notre perception de consommateur,le fait de mousser est tellement associé au fait de nettoyer, que l’industrie cosmétique ajoute dans ses produits certains agents amphiphiles servant surtout à mousser, plus qu’à nettoyer ! »
Bonne journée.
Voici les précisions que nous trouvons dans cet article du Figaro bien nommé : Pourquoi le savon mousse-t-il ? :
« Sans vouloir la faire mousser à mauvais escient, force est de reconnaître que
Science étonnante apporte de son côté une réponse complète à votre question en expliquant comment se comportent les molécules de savon et comment, au contact de l’air, elles créent des bulles (et donc de la mousse). Par ailleurs, cet article confirme qu’un savon naturel ou maison moussera moins qu’un savon industriel (sans pour autant que ses propriétés lavantes soient moindres) :
« le savon […] contient des
Grâce à cette propriété, les molécules amphiphiles peuvent alors emprisonner les graisses à la surface de notre peau (ou de nos assiettes), et permettre qu’on les élimine par un flux d’eau. […]
Comme vous avez pu le constater,
Tout d’abord, vous savez peut être qu’il n’y a pas vraiment besoin de savon pour faire des bulles. Si vous faites sortir rapidement de l’eau du robinet, vous pouvez constater que quelques bulles se forment brièvement, mais ont une durée de vie bien faible. Pas de quoi en faire une mousse.
La raison de la faible durée de vie de ces bulles, c’est que tout comme l’huile, l’eau et l’air ne s’aiment pas vraiment. Ils ont donc envie de minimiser leur interface; or une bulle est une grande surface d’interface entre l’eau et l’air. C’est pour cette raison que les bulles créées sans savon ne sont pas stables.
Mais de même que les molécules amphiphiles permettent de rendre compatibles l’eau et l’huile, elles permettent de conserver les bulles en réconciliant l’eau et l’air. Les molécules amphiphiles se placent à l’interface eau-air (la tête dans l’eau et la queue en l’air) et assurent la stabilité du mince film d’eau qui constitue la bulle.
L’image ci-contre représente ce qu’est une bulle, c’est-à-dire une double couche de molécules amphiphiles qui stabilisent un mince film d’eau. Attention tout cela n’est pas à l’échelle car le film d’eau ne fait que quelques dizaines de nanomètres d’épaisseur !

Et voilà pourquoi les produits nettoyants sont aussi inéluctablement des produits moussants ! En réalité, suivant leur structure, les molécules amphiphiles peuvent être plus efficaces à l’interface eau/huile (on parle alors de détergents) ou à l’interface eau/air (on parle alors d’agents moussants).
Mais dans notre perception de consommateur,
Bonne journée.
Pièces jointes
×
![]()
DANS NOS COLLECTIONS :
Ça pourrait vous intéresser :
Commentaires 0
Connectez-vous pour pouvoir commenter.
Se connecter



