Que siginifie la "VALENCE" des éléments?
SCIENCES ET TECHNIQUES
+ DE 2 ANS
Le 02/02/2016 à 23h22
878 vues
Question d'origine :
Bonjour, je n'arrive pas à comprendre lla signification et l'explication du terme "Valence" lorsque l'on dit: la valence des éléments fait partie des principes de classement du tableau périodique des éléments de Mendeleïv". Je ne saisis pas trop ce que cela veut dire.
Merci de votre réponse!
Réponse du Guichet
Le 05/02/2016 à 08h30
Bonjour,
En effet, depuis la nuit des temps, les hommes ont essayé de connaître les éléments constitutifs de notre Terre. Or, bien qu'il existe de nombreux éléments connus de l'homme,
source : Wikijunior
Autrement dit, le tableau périodique des éléments, également appelé table de Mendeleïev, classification périodique des éléments ou simplement tableau périodique, représente
La conception de ce tableau est généralement attribuée au chimiste russe Dmitri Mendeleïev, qui construisit en 1869 une table différente de celle qu'on utilise aujourd'hui mais similaire dans son principe, dont le grand intérêt était de proposer une classification systématique des éléments chimiques connus à l'époque en vue de souligner la périodicité de leurs propriétés chimiques, d'identifier les éléments qui restaient à découvrir, et même de pouvoir prédire les propriétés de ces éléments alors inconnus.
source : Wikipédia
La définition ci-dessus indique que
Nous supposons que vous savez déjà qu’un atome est constitué d’un noyau, lui-même constitué de protons (de charge électrique positive) et de neutrons (neutres électriquement) et d’un cortège d’électrons (de charge électrique négative).
La question qui se pose est la suivante : comment les électrons d’un atome sont-ils répartis autour du noyau ? Au début du XXe siècle, cette question a donné lieu à plusieurs théories successives. Il fallait aussi expliquer que les électrons de charge négative ne viennent pas s’écraser sur le noyau de charge positive… et qu’ainsi l’atome reste stable.
C’est ainsi que l’on nomme l’ensemble des Z électrons qui entourent le noyau. On dit aussi qu’il forme un « nuage électronique ». Il paraît évident que plus un électron est proche d’un noyau, plus il est solidement lié à celui-ci, plus il est stable. A l’inverse, un électron éloigné du noyau pourra être arraché à celui-ci par une action extérieure modérée, sa stabilité est moindre. Les électrons étant en perpétuel mouvement, chacun occupe un espace qui ne peut être réduit à sa seule dimension. De ce fait, tous les électrons ne peuvent être au plus prêt du noyau dans une position de stabilité maximale.
Pour désigner les différentes couches électroniques d’un atome, on utilise les lettres K, L, M…
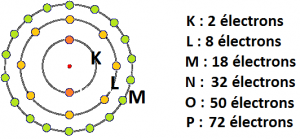
Source : physiquereussite.fr
La dernière couche occupée par les électrons est dite couche externe ou couche périphérique. […]
Source : Matière et énergie dans les systèmes : manuel de chimie-biochimie alimentaire
On définit ainsi la valence d'un élément, par le nombre d'électrons célibataires. Connaître la valence d'un élément permet de savoir comment il peut se lier.
Source : Cours de chimie et d'électricité : CAP coiffure CAP esthétique
Lorsque l’on classe les atomes par ordre atomique Z croissant, on constate une périodicité au niveau de la couche électronique externe. Si l’on place dans une même colonne les atomes ayant le même nombre d’électrons sur leur couche externe, l’ensemble se répartit sur 18 colonnes (dont 8 principales) et 7 lignes, chacune se terminant par un atome possédant 8 électrons sur sa couche externe.[…]
Source : Matière et énergie dans les systèmes : manuel de chimie-biochimie alimentaire
Graphiquement, on peut représenter les éléments en ne retenant que leur nombre de valence :

Source : Les électrons de valence par Science François Eduardo, projet scolaire canadien.
Les éléments d’une même colonne possédant des propriétés semblables. Ils sont classés en famille dont certaines portent un nom particulier.[…]
Ainsi l’atome d’azote (noté N) possède 5 électrons sur sa couche externe et cherchera à mettre en commun 3 électrons pour parvenir à remplir totalement sa couche externe, soient 8 électrons, tandis que l’Oxygène, placé juste à sa droite, avec donc un électron supplémentaire par rapport à l’azote, avec 6 électrons sur sa couche externe, mettra en commun 2 électrons pour parvenir à remplir totalement sa couche externe, soient 8 électrons.
Source :
Matière et énergie dans les systèmes : manuel de chimie-biochimie alimentaire
*
*
Source : Le Repaire des Sciences
Pour en savoir plus sur l'histoire du tableau périodique :
- La classification périodique de Lavoisier à Mendeleïev, de CultureSciencesChimie par l'ENS de Cachan
- Le roman des éléments de I. Nechaev & G. Jenkins
- La classification périodique des éléments : la merveille fondamentale de l'Univers de Paul Depovere
Commentaires 0
Connectez-vous pour pouvoir commenter.
Se connecter



 Barbès blues
Barbès blues